Группа исследователей из Института биоорганической химии имени академиков М.М. Шемякина и Ю.А. Овчинникова РАН и МГУ имени Ломоносова совместно с Университетом Юты при помощи метода FRET-микроскопии впервые показала способность нуклеосом обратимо раскручиваться под воздействием белкового комплекса FAСT без затрат энергии. В дальнейшем полученные данные помогут понять, какую роль этот белковый комплекс играет в активно делящихся клетках в опухолевых тканях. Об исследовании сообщается в пресс-релизе ИБХ РАН.
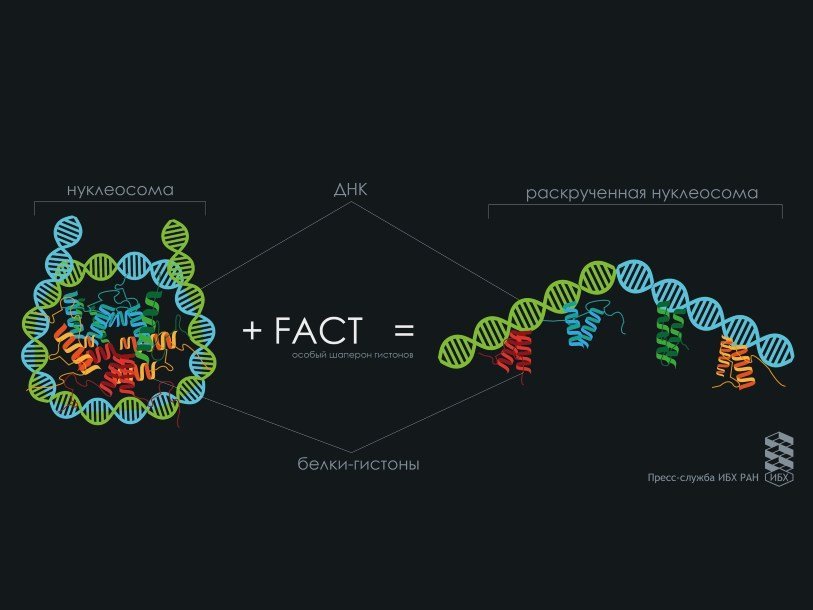
Как известно, молекула ДНК компактно свернута в ядрах клеток. Правильность укладки генома обеспечивают специальные белки, которые вместе с ДНК формируют структуру под названием хроматин. Единицей компактизации хроматина является нуклеосома. Нуклеосому часто сравнивают с «катушкой ниток», в которой ДНК-«нитка» намотана на бочонок из белков-гистонов – «катушку». Плотная упаковка хроматина в ядре нарушается при транскрипции, когда идет считывание наследственной информации с ДНК. Облегчить транскрипцию хроматина помогает консервативный белок FACT. Взаимодействие FACT с нуклеосомой было отмечено ранее, но впервые удалось выяснить важные детали этого процесса. Исследователи изучили взаимодействие белкового фактора FACT с нуклеосомой методом spFRET-микроскопии.
Данная работа является примером успешного сотрудничества между двумя научными группами, – рассказывает Ксения Кудряшова, кандидат биологических наук, научный сотрудник Отдела биоинженерии ИБХ РАН. – Первую группу возглавляет исследователь нуклеосом с большим стажем Василий Михайлович Студитский, заведующий лабораторией регуляции транскрипции и репликации МГУ. Вторая научная группа проводила исследования под руководством специалиста по микроскопических методам в биологии Алексея Валерьевича Феофанова, руководителя лаборатории оптической микроскопии и спектроскопии биомолекул ИБХ РАН».
«В результате начатой еще в 2010 году плодотворной работы удалось с нуля разработать метод spFRET и применить его для исследования нуклеосом, – объясняет Ксения Кудряшова. – Его основу составляет микроскопия единичных молекул. В соседние витки нуклеосомной ДНК вводятся флуоресцентные метки, одна из которых служит донором энергии, а другая – акцептором. Донора можно возбудить с помощью лазера определенной длины волны. Если донор находится близко к акцептору, то происходит переброс энергии на акцептор. Чем ближе расположены метки, тем ярче сигнал от акцептора. Таким образом, можно следить за расстоянием между соседними витками ДНК и оценивать, насколько нуклеосома компактно свернута. Это уникальная для России разработка. Она позволяет изучать структурные перестройки в нуклеосомных комплексах с разрешением в несколько нанометров, причем информация собирается от каждой молекулы индивидуально».
С использованием этого метода в работе впервые показали способность нуклеосом обратимо раскручиваться под воздействием FACT in vitro без затрат энергии, что достаточно необычно. Ведь АТФ-зависимые комплексы ремоделирования для перестройки хроматина тратят много энергии. При образовании комплекса «нуклеосома-FACT» нити ДНК практически полностью распрямляются, но остаются связанными с белками-гистонами. Если убрать FACT из комплекса, то все возвращается на круги своя: нуклеосомная ДНК снова наматывается на основание из гистонов. Таким образом, FACT – это редкий пример АТФ-независимого (без естественных источников энергии) комплекса ремоделирования хроматина.
По мнению Марии Валиевой, первого автора статьи из МГУ, в клетке способность FACT обратимо менять структуру хроматина, возможно, помогает активировать определенные гены путем перестройки соответствующих участков ДНК. Однако ничего более конкретного нельзя сказать о подобных процессах, происходящих в клетках, так как вопрос еще недостаточно изучен. Автор отмечает, что изучение этого белкового комплекса важно не только с научной, но и медицинской точки зрения. Это связано с тем, что FACT в большом количестве содержится в опухолевых тканях. Именно поэтому перед учеными стоит вопрос: «Какую роль этот белковый комплекс играет в активно делящихся клетках?».
Результаты работы опубликованы в журнале Nature Structural & Molecular Biology.